“《德国药剂师报》(Deutsche Apotheker Zeitung)表示,目前尚不清楚更低剂量的药物暴露在降低副作用风险方面效果有多大。由于患者数量有限,因此很难得出可靠的结论。”
2023年3月20日
亲爱的朋友们:
德国历史最悠久、最畅销的医药期刊对非那雄胺后综合征(PFS)进行了深入研究。
 目的是为了向其29000名订阅者提供关于未经FDA批准的外用非那雄胺的最科学、可靠的信息。
目的是为了向其29000名订阅者提供关于未经FDA批准的外用非那雄胺的最科学、可靠的信息。
在此之前,又有一个国家将外用非那雄胺作为口服制剂的“更安全”替代品推向市场。
明天,韩国制药公司Boryung (003850.KS)在韩国食品和药物安全部的批准下,将在韩国推出Finjuve非那雄胺喷雾剂。Finjuve由英国Hikma制药公司(LSE: HIK)生产,现已在德国、意大利、葡萄牙和卢森堡获得批准。
尽职调查
由Tony Daubitz博士撰写的题为《副作用:生发的后果》(英文摘要)的2000字分析于3月10日发表在《德国药剂师报》(DAZ)上,距其关于此问题的第一篇报道《外用非那雄胺是治疗脱发的更好选择吗?(英语)》仅一个月。
在柏林Max Delbrück分子医学中心获得博士学位的Daubitz博士引用了28项临床研究,其中许多作者对于本新闻提要的读者来说无疑非常熟悉,包括:
米兰大学的Roberto Cosimo Melcangi博士,贝勒医学院的Mohit Khera博士,哈佛医学院的Michael S. Irwig博士,波士顿大学医学院的Abdulmaged M. Traish博士。
他还在已发表的病例报告中提供了以下17种PFS症状的图表:
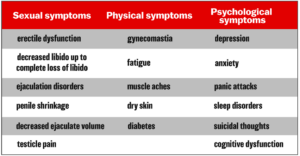 在罗列出证据支持所有服用口服非那雄胺的患者中有一部分会出现PFS的假设后,Daubitz博士写道:
在罗列出证据支持所有服用口服非那雄胺的患者中有一部分会出现PFS的假设后,Daubitz博士写道:
一种新的(口服非那雄胺)替代治疗方案外用非那雄胺(Fynzur, 2275 mg/ml)最近在德国推出。在一项涉及250名志愿者的III期研究中[外用非那雄胺喷雾剂治疗男性雄激素性脱发的疗效和安全性],该喷雾剂显著刺激毛发生长……并显示出与口服非那雄胺类似的效果……另一方面,外用型药物的暴露不足口服的百分之一。血液中的二氢睾酮水平也相应地下降至更低,这就是为什么预期副作用更小的原因。
谨慎行事
所以外用非那雄胺更安全,对吧?就这样了,对吗?Daubitz博士写道:
通过对药物的分析,乍一看似乎很有希望的事情却有了不同的看法。目前还不能说外用解决方案的效果是否真的等同于片剂,因为这项研究并不是为了统计评估此而设计。而这仅仅是部分不足之处。只有71%的受试者完成了研究,只有55%的受试者有可评估的照片来评估治疗是否成功。
在[联邦药物和医疗器械研究所]委托进行的响应者分析中,受试者还被要求自己对脱发的改善情况进行评分。然而,在主观评估上没有显著差异(外用非那雄胺组39.8%的男性头发生长得到改善,口服非那雄胺组31.0%,安慰剂组32.0%)。
然后他总结道:
目前尚不清楚更低剂量的药物暴露在降低副作用风险方面效果有多大。尽管性方面副作用的报道并没有比安慰剂更频繁……但正如Arznei-Telegramm所指出的那样,研究中患者数量有限,很难得出可靠的结论。尽管如此,预测这种副作用的发生还是很重要的。
Hims日益臭名昭著
然而,在Daubitz博士署名之前,他指出:
虽然外用非那雄胺在美国没有被批准作为药品,但它却通过ForHims.com等远程医疗门户网站作为非处方药品销售。当DAZ编辑问及这一点时,非那雄胺后综合征基金会指出,他们知道有许多病例是由外用非那雄胺引起的。因此迫切需要对该综合征进行进一步的研究。
更真实的文字从未透露。上个月我们公开,迄今为止,已有12名PFS患者向我们提交病例报告,表明他们在只使用外用非那雄胺后就出现了这种症状(德国顶级药学期刊警告,外用非那雄胺可能导致PFS)。
第一个公开的案例是来自芝加哥的21岁大学生Sumair Ahluwalia,他在使用Hims执业护士Charlene Fernandez为他开的外用非那雄胺和米诺地尔喷雾剂的处方后不久就出现了全面的PFS。
Daubitz博士提到Hims & Hers Health (NYSE: HIMS)标志着几个月来这家总部位于旧金山的远程医疗公司第二次在欧洲媒体报道中被单独提到,这家公司还在英国销售口服和外用非那雄胺。
3月4日,《每日邮报》发表了一篇题为“监管机构对脱发药物展开调查,因为男性报告包括抑郁、性欲低下和勃起功能障碍在内的副作用的案例大幅上升”的报道。它的副标题是:“数据显示,Hims等品牌销售的脱发治疗药物的副作用正在上升。”
 对我们来说,非那雄胺患者在接受Hims或其他远程医疗公司的处方后报告患上PFS的案例越来越多,这是我们记载了五年的数据。正如我们在2018年年度致词中所指出的:
对我们来说,非那雄胺患者在接受Hims或其他远程医疗公司的处方后报告患上PFS的案例越来越多,这是我们记载了五年的数据。正如我们在2018年年度致词中所指出的:
美国加州圣何塞市的眼科外科医生Keshav Narain联系我们说:“我最近看到一位使用非那雄胺的病人。他没有处方就通过Hims拿到了这种药。我相信这些人中的绝大多数都不知道这种药物的潜在危险。除了已知的雄激素阻断所导致的副作用,我们相信一部分患者最终会出现神经方面的症状。”
18个月后,也就是2020年3月,我们在《华尔街日报》的观点版面上写道:
平均每个月有45名新PFS患者从全球各地敲开我们的数字大门,自2018年以来,这一数字增长了462%……越来越多的患者告诉我们,实际上是Hims、Keeps或Roman给他们开的非那雄胺。而且几乎没有PFS方面的警告。
就在七个月前,在一篇题为“应FDA要求,美国保法止产品标签上首次添加自杀倾向不良反应”的报道中,我们写道:
更大的问题(在确保所有服用非那雄胺1mg或考虑服用非那雄胺1mg的美国患者立即被告知FDA已经承认该药物可能导致自杀方面)在于三大远程医疗服务公司的核心业务至少部分是非那雄胺销售占主导地位。
自2017年成立以来,Hims、Keeps和Ro(前身为Roman)已经筹集了约13亿美元的风险投资,这让他们有足够的资金来积极瞄准寻求脱发治疗的男性。问题是,根据PFS基金会对这三家远程医疗机构的消费者数字内容的审查,没有一家(提到FDA强制要求的)自杀倾向药物不良反应报告。
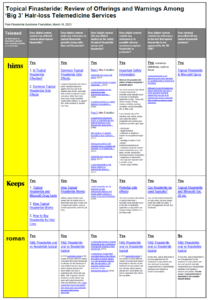
现在,随着更多关于PFS患者仅使用外用非那雄胺就导致患病的报道,我们对该研究进行了补充:外用非那雄胺:回顾“三大”脱发远程医疗服务公司提供的产品和警告。
最显著的结果是,与竞争对手Hims和Keeps不同,Ro选择不销售外用非那雄胺产品或者不开外用非那雄胺产品的处方。其理由很简单:
目前,外用非那雄胺还没有被FDA批准用于治疗男性型脱发,必须由配制药房专门配制,并需要医生的处方。因此,配制外用非那雄胺无法通过Roman获得。
与此同时,Keeps似乎尚未决心确定外用非那雄胺比口服非那雄胺更好还是更差。
一方面,其主页上唯一的产品是外用非那雄胺和米诺地尔凝胶,因此宣传:“保持发量从未如此简单。每天使用一次的啫喱里就有两种经过临床验证的产品。”
另一方面,它的外用非那雄胺和米诺地尔药物介绍页面形同虚设。除了标题中的“外用非那雄胺”一词外,该页对外用非那雄胺的提及为零。而且该页面上引用的两项与非那雄胺相关的临床研究分别发表于1998年和1999年,比外用非那雄胺作为雄激素性脱发(AGA)的可能疗法首次出现在医学文献中早了十多年。
更奇怪的是,在Keeps的另一个题为“如何购买非那雄胺治疗脱发”的网页中,有一节的标题是“非那雄胺可以外用吗?”,部分内容如下:
您可以在网上找到外用非那雄胺,但您应该注意,与药片不同,它没有被FDA批准用于治疗脱发……如果未来有更多正面的研究结果,FDA可能会考虑改变其对外用非那雄胺的立场。在那之前,为了保险起见,我们建议大家还是坚持口服。
所以还是药片,对吧?没那么快。
任何想要服用非那雄胺的患者,如果有必要的资金,可以在Keeps的非那雄胺页面上找到该药物的处方信息(PI)链接。问题是,自从五个月前我们对美国FDA规定的自杀倾向不良反应披露进行审查以来,Keeps更新了该页面,使用了最新版本的处方信息,现在将“自杀倾向和行为”列为不良反应。
很难想象有比自杀更糟的不良反应了。但从Keeps的数字消费内容的“逻辑”来看,它的每瓶外用非那雄胺和米诺地尔凝胶里,都可能暗藏风险。
至于Hims,我们在上个月就亲眼目睹了它的外用非那雄胺处方流程。然而,值得一提的是,这家市值20亿美元的公司将外用非那雄胺&米诺地尔喷雾剂作为其“客户首选”和“最受欢迎”的产品。
由于FDA不评论正在考虑上市批准(与否)的产品,我们通过该机构的网站筛选有关外用非那雄胺在美国未来状态的线索。在监管方面,我们发现了两个案例:
- Hybrid Pharma LLC:2021年在佛罗里达州迪尔菲尔德海滩的检查,外包设施(又名配制设施)的检查结果如下:
你们的外包工厂在最初注册为外包工厂时没有向FDA提交报告,说明前六个月期间配制的药物。具体地说,以下产品是配制的,没有在你们的报告中说明:米诺地尔5%,维甲酸0.01%,非那雄胺2.5%外用溶液……
- Rx Unlimited Pharmacy:2022年在加利福尼亚州 North Hills的外包设施进行检查的结果如下:
自2022年5月以来,你们公司生产了使用[经过修改]作为成分的[经过修改]药品配方(鼻喷雾剂、口服混悬液、口服和外用溶液)。在过去三个月里,你们公司配发了含有[经过修改]作为成分的[经过修改]患者处方。例如,你们配发了以下配制药产品:
– 非那雄胺泡沫0.2%
– 米诺地尔6%/非那雄胺0.2%外用溶液
所以我们知道FDA正在关注外用非那雄胺产品的生产和配药。但根据2023年3月14日的最新报告,非那雄胺目前正在作为一种用于配制的“原料药”进行评估。
当Roman Kulikov得知外用非那雄胺已在德国和韩国获得批准后,他立即站出来为全球PFS患者发声。
这位来自柏林的32岁厨师说:“我们在1997年就被保法止药片骗了,26年后的今天,我们又在被这些非那雄胺霜剂、凝胶和喷雾剂欺骗。”自2015年以来,他一直患有PFS。
他补充道:“我们以为默克(Merck)和欧加农(Organon)这样的制药公司在推进科学发展,但实际上他们不过是想着自己的银行账户。”
Ro越来越渴望从他的40多种PFS症状中解脱出来——从阴茎萎缩到男性乳房发育,从牙齿脱落到血糖升高,从肌肉萎缩到极端情绪波动——三年前,他求助于Münster生殖医学和男科中心的Michael Zitzmann医学博士。
“患者在2015年服用了3个月的非那雄胺……患者担心他的阴茎可能会消失。有时感觉不到这个器官的存在。这次没有关系。不想要亲子关系,”齐茨曼博士在Ro的病例中写道。他在2018年接受《DAZ》采访时的标题是“靶向神经活性类固醇”。
“我的认知能力大大下降,我的智商也下降了,”Roman说。“我曾经能够独立思考,轻松处理复杂的任务。但现在,即使是最简单的智力挑战,我也难以应对。”
 任何居住在美国并患有非那雄胺后综合征的人都应该向美国FDA报告其症状。任何居住在美国以外并患有非那雄胺后综合征的人都应该向美国FDA以及其当地的药品监管机构报告其症状,正如我们的“举报你的副作用/Report Your Side Effects”页面所示的那样。
任何居住在美国并患有非那雄胺后综合征的人都应该向美国FDA报告其症状。任何居住在美国以外并患有非那雄胺后综合征的人都应该向美国FDA以及其当地的药品监管机构报告其症状,正如我们的“举报你的副作用/Report Your Side Effects”页面所示的那样。
最后,如果您或您爱的人正在遭受非那雄胺后综合征,特别是感到抑郁或情绪不稳定,请不要犹豫,尽快通过我们的患者支持热线联系我们:social@pfsfoundation.org
谢谢!
相关新闻