16 сентября 2019 г.
Дорогие друзья:
 Дэн Левайн, журналист-расследователь крупнейшего информационного агентства в западном мире, на прошлой неделе опубликовал отчет о расследовании из 3900 слов под заголовком «Суд разрешил Мерк скрывать секреты о рисках, связанных с популярным лекарством».
Дэн Левайн, журналист-расследователь крупнейшего информационного агентства в западном мире, на прошлой неделе опубликовал отчет о расследовании из 3900 слов под заголовком «Суд разрешил Мерк скрывать секреты о рисках, связанных с популярным лекарством».
Год спустя история Reuters раскрыла показания бывших руководителей Merck в судебном процессе в США по Пропеции, свидетельствующие о том, что фармацевтический гигант преуменьшал побочные эффекты препарата во время клинических испытаний.
Эта история является частью более широкой серии расследований, посвященных десятилетней тенденции судебных органов в делах об ответственности за качество продукции, которые запечатлевают доказательства, которые в противном случае могли бы помочь предотвратить кризисы в области общественного здравоохранения и безопасности.
В результате такой секретности, отмечает Reuters, «сотни тысяч американцев были убиты или серьезно ранены якобы дефектными продуктами», включая лекарства, медицинские приборы и автомобили.
Расследование Конгресса
Объявленный как «Скрытая несправедливость», серия Reuters стартовала 25 июня с докладом «Как судьи добавили к мрачному количеству опиоидов, который быстро вызвал действие на Капитолийском холме».
26 сентября подкомитет Судебного комитета Палаты представителей США заслушает показания об отсутствии ясности в наших федеральных судах, при этом основное внимание будет уделено судьям, которые, как известно, скрывают важные документы, и при этом игнорируют закон США, который предусматривает суд документы должны быть публичными.
Хэнк Джонсон, конгрессмен-демократ из Грузии, на прошлой неделе заявил агентству Reuters, что расследование призвано пролить свет на этот вопрос, поэтому судьи добровольно принимают меры для соблюдения прецедентного права. «Если они этого не сделают, — сказал он, — тогда законодательство может приступить к процессу».
Среди тех, кто дает показания перед Конгрессом, будет Левин, репортер, ответственный за то, что он обнаружил доказательства того, что Мерк скрывает секреты своих рецептурных средств от выпадения волос, которые с 1997 года назначаются миллионам мужчин, включая президента Дональда Трампа.
Толчок для полного раскрытия
 На следующий день после того, как репортаж Левина попал на новостные ленты по всему миру, Reuters подало в федеральный суд ходатайство о раскрытии документов, поданных в ходе судебного разбирательства по делу о массовом гражданском правонарушении касательно Пропеции, которые раскрывают потенциальные риски, связанные с наркотиками. Движение относится к одному из четырех случаев «вожак».
На следующий день после того, как репортаж Левина попал на новостные ленты по всему миру, Reuters подало в федеральный суд ходатайство о раскрытии документов, поданных в ходе судебного разбирательства по делу о массовом гражданском правонарушении касательно Пропеции, которые раскрывают потенциальные риски, связанные с наркотиками. Движение относится к одному из четырех случаев «вожак».
«Это случай огромной важности, который был закрыт без официальной информации, объясняющей это закрытие. Первая поправка исключает такой исход», — утверждает Reuters.
«Эти документы важны не только для собственных расследований Reuters о Пропеции, но и для широкой общественности, которая продолжает принимать это лекарство, и врачей, которые продолжают назначать его пациентам».
Ссылаясь на отчет Левина, в предложении поясняется, что хотя скрытые документы, включая показания бывших руководителей Merck, были частично отредактированы, «Reuters удалось просмотреть затемненный материал после копирования его из цифровой версии движения и вставки его в документ в другой формат.»
В одном из таких документов Кейт Кауфман, доктор медицинских наук, руководитель программы клинического развития Пропеция, обсудил альтернативные способы интерпретации данных клинических испытаний. Ссылаясь на формулировку на этикетке Пропеции, в которой говорится, что из тех мужчин, которые принимали препарат в течение всех пяти лет «не более 0,3%», страдали сексуальными побочными эффектами к пятому году, он назвал эту цифру «полностью вводящей в заблуждение». Потому что к пятому году «вы отсеяли выбывших из-за сексуальных [неблагоприятных переживаний]».
Гражданская петиция Фонда ПФС
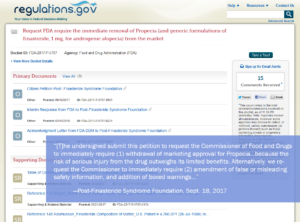 В ходе своего расследования Левин также обнаружил петицию граждан, которую Фонд ПФС подал в Управление по контролю за продуктами и лекарствами США два года назад, с требованием, чтобы агентство «немедленно потребовало отзыва маркетингового одобрения для Пропеции… потому что риск серьезных травм от препарата перевешивает его ограниченные преимущества ».
В ходе своего расследования Левин также обнаружил петицию граждан, которую Фонд ПФС подал в Управление по контролю за продуктами и лекарствами США два года назад, с требованием, чтобы агентство «немедленно потребовало отзыва маркетингового одобрения для Пропеции… потому что риск серьезных травм от препарата перевешивает его ограниченные преимущества ».
В качестве альтернативы мы попросили, чтобы (a) в упаковке продукта Пропеция были указаны предупреждения, меры предосторожности и противопоказания в каждой упаковке касательно серьезных рисков, связанных с лекарственным средством, включая стойкую эректильную дисфункцию, серьезное депрессивное расстройство и мужское бесплодие, (b) заставить FDA пересмотреть маркировки других значительных продуктов и (c) FDA требует от Мерк разработать и внедрить план стратегии оценки и смягчения рисков.
«Открытое и закрытое» свидетельство
Среди судебных документов, которые Левин также обнаружил и впоследствии опубликовал вместе со своим отчетом, есть ходатайство, поданное Исполнительным комитетом истцов, наряду с экспонатами свидетельских показаний бывшего руководителя Мерк, Шарлотты Мерритт, которая курировала регулирующую деятельность для Пропеции, и Пол Хоуз, который возглавлял маркетинг для препарата.
Как объясняет Левин, эти документы первоначально были «открыто поданы в федеральный суд. Год спустя адвокаты сказали судье, что они собирались подать [их] под печатью, и она согласилась опечатать [их] без объяснения причин».
Ниже приводятся выдержки из показаний Мерритта и Хоуза в 2016 году:
— Когда его спросили, почему в своей редакции 2002 года на этикетке продукта Мерк изменил фразу «Разрешение произошло у всех мужчин, которые прекратили терапию с помощью Пропеции…», на «Разрешение произошло у мужчин, которые прекратили терапию с помощью Пропеции», Мерритт сказал:
«Ну, как вы видели, были некоторые мужчины, у которых через некоторое время [сексуальные неблагоприятные события] не разрешились, так что слово « все » больше не было фактическим, поскольку относится к более долгосрочным данным после начального периода испытания».
— Когда спросили, не мешает ли что-то Мерк, опять же в пересмотренной редакции своего продукта 2002 года, раскрыть данные, которые они держали в течение более года на тот момент, о мужчинах в клинических испытаниях, «продолжающих испытывать сексуальные нежелательные явления после прекращения» наркотик, Мерритт сказал:
«В то время Мерк не чувствовал, что это должно быть что-то, что должно быть помещено на этикетке».
— Когда в «Пересмотре товарного знака» от 2002 года был задан вопрос: «Мерк мог бы… прояснить, что были случаи, когда у пациентов развивались сексуальные побочные эффекты в… клинических испытаниях, у которых сексуальные побочные эффекты не прекращались после прекращения лечения»? Мерритт сказал:
«Это могло бы быть сделано, если бы Мерк считал, что это было бы подходящим способом обозначить на основе данных. Я не могу комментировать почему — почему это было сделано так, как это было сделано».
—Ссылаясь на внутреннюю публикацию Мерк под названием «Оценка рекламной кампании 1998 года для потребителей, посвященной потребителям, Отчет об исследовании осведомленности потребителей и действиях на конец года», датированный 15 марта 1999 г., Хоуса спросили: Стоит ли полагать, что если бы 20% мужчин, которые были в группе парней, которые могли использовать препарат, не трогали бы его, признавая, что симптомы могут исчезнуть, то этот процент был бы еще выше, если бы они думали, что использование препарата может вызвать постоянные проблемы для них?» Хоус ответил:
«Да.»
— Когда мы снова обратились к вышеупомянутому исследованию, спросили: «Итак, выход из этого состоял в том, что мы понимаем, что у нас есть проблема с сексуальными побочными эффектами, и мы, как компания, должны выяснить, как решить эту проблему?» Хоус сказал:
«Да.»
 Любой, кто живет в США и страдает от PFS должен сообщить о своих симптомах в Управление США по надзору за качеством пищевых продуктов и лекарственных средств (FDA or USFDA).
Любой, кто живет в США и страдает от PFS должен сообщить о своих симптомах в Управление США по надзору за качеством пищевых продуктов и лекарственных средств (FDA or USFDA).
Любой, кто живет за пределами США и страдает от PFS, должен сообщить о своих симптомах в Управление по контролю за продуктами и лекарствами США (FDA or USFDA), а также в свое национальное агентство по контролю над наркотиками, как указано на нашей странице «Сообщить о ваших побочных эффектах».
В заключение, если вы или ваш близкий человек страдаете от PFS, и Вы чувствуете себя подавленным или нестабильным, пожалуйста, не стесняйтесь обращаться в Фонд PFS как можно скорее через нашу горячую линию поддержки пациентов: social@pfsfoundation.org
Спасибо.
